Anolyte: potente biocida
Due sono le soluzioni Anolyte prodotte: Anolyte Acido e Anolyte neutro.
Di seguito è possibile valutarne le differenze:
Il Cloro Attivo, contenuto nell’Anolyte, è l’elemento biocida/battericida. La sua concentrazione è la medesima nelle due soluzioni e l'unica differenza è il valore del pH. Quindi in tutte le applicazioni in cui vi è la problematica della corrosione è meglio utilizzare l'Anolyte Neutra.
Inoltre non vi è formazione significativa di composti di cloro da contatto organico, come ad esempio i trialometani e non vi è nemmeno nessun sottoprodotto tossico da contatto inorganico quali Cloriti (ClO2) e Clorati (ClO3).
Come si può notare dalla tabella, i principali composti che si sviluppano all'interno del reattore sono l'acido ipocloroso e lo ione ipoclorito. Le percentuali non sono definite in quanto la loro somma è pari allo 0.05% del volume, e sono legate al valore del pH della soluzione come si può notare nell'immagine successiva.
Il grafico mostra una predominanza dell'acido ipocloroso HClO, quando i valori di pH sono inferiori al 7.5, mentre quando i valori di pH sono superiori si ha una predominanza dello ione ipoclorito ClO-.
Dal momento che l’effetto germicida del HClO è molto più alto (80-120 volte) di quello degli ioni ClO- è preferibile la clorazione a pH basso che comporta predominanza di acido ipocloroso (HClO).
Oltre a questi, in percentuali molto piccole si sviluppano anche: ClO2, HClO3, HClO4, H2O2, O2, ClO2-, ClO3-, O-, HO2-, OH-.
Tutti questi componenti permettono di rendere l'Anolyte Neutro un potente agente battericida e sporicida.
Cl2(g) + H2O --------> HClO + H+ + Cl-
L’acido ipocloroso è debole e si dissocia facilmente in ioni di idrogeno e di ioni ipoclorito, come si nota nella reazione 2:
HClO <---> H+ + OCl- (2)
Quando viene sciolto in acqua si sviluppa la seguente reazione:
NaOCl + H2O -------> HClO + Na+ + OH-
Quindi l’aggiunta di sodio ipoclorito all’acqua produce acido ipocloroso, similarmente all’idrolisi del cloro gassoso.
Dal momento che l’aggiunta di ipoclorito di sodio all’acqua produce ioni idrossili che aumentano il pH dell’acqua e che un eventuale eccesso di idrossido di sodio aumenta ulteriormente il pH dell’acqua, l'uso dell'ipoclorito di sodio per la disinfezione diventa problematico, considerando anche la necessità di utilizzare componenti chimici sia per la produzione che per la stabilizzazione della soluzione.
La reazione tra il calcio ipoclorito e l’acqua è indicato nella reazione seguente:
Ca(OCl)2 + 2H2O -------> 2HClO + Ca++ + 2OH-
Dalla reazione si nota che l’utilizzo di ipoclorito di calcio nell’acqua produce anche acido ipocloroso, come nell’idrolisi del cloro gassoso.
Similarmente alla soluzione di sodio ipoclorito, l’aggiunta di calcio ipoclorito libera ioni idrossili che aumentano il pH dell’acqua.
Innanzitutto, essendo a ph 7 garantisce che la proporzione tra acido ipocloroso e ione ipoclorito sia nettamente spostata verso l'acido ipocloroso, 80% contro il 20% di ione ipoclorito, garantendo un elevato potere battericida.
Il reattore produce gli stessi principi biocidi (HClO e ClO-) degli altri agenti disinfettanti ma ha numerosi vantaggi: non è tossico, nè corrosivo, nè pericoloso, non induce resistenza nei batteri ed elimina/limita la formazione di sostanze indesiderate (THMs, Cloriti, Clorati, ...).
Inoltre imitando il funzionamento del sistema immunitario, o meglio, imitando il comportamento dei leucociti (neutrofili, macrofagi) risulta essere particolarmente efficace.
Infatti le cellule estranee vengono dapprima fagocitate e poi distrutte grazie all'azione dell'acido ipocloroso (HClO), agente biocida prodotto da un enzima, la mieloperossidasi (MPO), a partire dal perossido di idrogeno (H2O2) e ioni di cloruro Cl-, durante l'esplosione ossidativa (respiratory burst).

Di seguito è possibile valutarne le differenze:
| pH | ORP (mv) | Active Chlorine (mg/l) | |
|---|---|---|---|
| Anolyte acido | 2.0 - 3.5 | 1000-1200 | 500 - 700 |
| Anolyte Neutro | 5.5 - 8.5 | 700 - 900 | 500 - 700 |
Inoltre non vi è formazione significativa di composti di cloro da contatto organico, come ad esempio i trialometani e non vi è nemmeno nessun sottoprodotto tossico da contatto inorganico quali Cloriti (ClO2) e Clorati (ClO3).
Composizione dell'Anolyte
| Componente | Simbolo | Volume | N° EINECS |
|---|---|---|---|
| Acqua | H2O | 99.69% | 231-791-2 |
| Cloruro di sodio | NaCl | 0.26% | 231-598-3 |
| Acido ipocloroso Ione ipoclorito |
HClO ClO- |
0.05% | 231-959-5 231-668-3 |
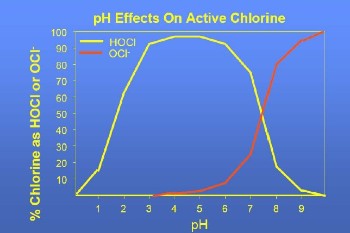
Il grafico mostra una predominanza dell'acido ipocloroso HClO, quando i valori di pH sono inferiori al 7.5, mentre quando i valori di pH sono superiori si ha una predominanza dello ione ipoclorito ClO-.
Dal momento che l’effetto germicida del HClO è molto più alto (80-120 volte) di quello degli ioni ClO- è preferibile la clorazione a pH basso che comporta predominanza di acido ipocloroso (HClO).
Oltre a questi, in percentuali molto piccole si sviluppano anche: ClO2, HClO3, HClO4, H2O2, O2, ClO2-, ClO3-, O-, HO2-, OH-.
Tutti questi componenti permettono di rendere l'Anolyte Neutro un potente agente battericida e sporicida.
Come si ottiene tradizionalmente il Cloro?
Gas di Cloro
Il gas di cloro si idrolizza rapidamente nell’acqua per formare acido ipocloroso (HClO) con la seguente reazione di idrolisi:Cl2(g) + H2O --------> HClO + H+ + Cl-
L’acido ipocloroso è debole e si dissocia facilmente in ioni di idrogeno e di ioni ipoclorito, come si nota nella reazione 2:
HClO <---> H+ + OCl- (2)
Ipoclorito di Sodio
Il cloro può essere ottenuto anche dall'ipoclorito di sodio, che contiene cloro in una concentrazione del 12.5%.Quando viene sciolto in acqua si sviluppa la seguente reazione:
NaOCl + H2O -------> HClO + Na+ + OH-
Quindi l’aggiunta di sodio ipoclorito all’acqua produce acido ipocloroso, similarmente all’idrolisi del cloro gassoso.
Dal momento che l’aggiunta di ipoclorito di sodio all’acqua produce ioni idrossili che aumentano il pH dell’acqua e che un eventuale eccesso di idrossido di sodio aumenta ulteriormente il pH dell’acqua, l'uso dell'ipoclorito di sodio per la disinfezione diventa problematico, considerando anche la necessità di utilizzare componenti chimici sia per la produzione che per la stabilizzazione della soluzione.
Ipoclorito di Calcio
Il calcio ipoclorito in commercio contiene normalmente il 65 percento di cloro disponibile.La reazione tra il calcio ipoclorito e l’acqua è indicato nella reazione seguente:
Ca(OCl)2 + 2H2O -------> 2HClO + Ca++ + 2OH-
Dalla reazione si nota che l’utilizzo di ipoclorito di calcio nell’acqua produce anche acido ipocloroso, come nell’idrolisi del cloro gassoso.
Similarmente alla soluzione di sodio ipoclorito, l’aggiunta di calcio ipoclorito libera ioni idrossili che aumentano il pH dell’acqua.
Come si può ottenere del Cloro in modo biologico?
Anolyte neutro
La soluzione di Anolyte neutro essendo a pH 7 consente di risolvere molti dei problemi legati alla generazione di acido ipocloroso.Innanzitutto, essendo a ph 7 garantisce che la proporzione tra acido ipocloroso e ione ipoclorito sia nettamente spostata verso l'acido ipocloroso, 80% contro il 20% di ione ipoclorito, garantendo un elevato potere battericida.
Il reattore produce gli stessi principi biocidi (HClO e ClO-) degli altri agenti disinfettanti ma ha numerosi vantaggi: non è tossico, nè corrosivo, nè pericoloso, non induce resistenza nei batteri ed elimina/limita la formazione di sostanze indesiderate (THMs, Cloriti, Clorati, ...).
Inoltre imitando il funzionamento del sistema immunitario, o meglio, imitando il comportamento dei leucociti (neutrofili, macrofagi) risulta essere particolarmente efficace.
Infatti le cellule estranee vengono dapprima fagocitate e poi distrutte grazie all'azione dell'acido ipocloroso (HClO), agente biocida prodotto da un enzima, la mieloperossidasi (MPO), a partire dal perossido di idrogeno (H2O2) e ioni di cloruro Cl-, durante l'esplosione ossidativa (respiratory burst).




